??? 隨著2021年醫(yī)療器械注冊人制度的全面實施�,醫(yī)療器械跨區(qū)域委托生產(chǎn)逐漸成為常態(tài)�����,在極大促進產(chǎn)業(yè)發(fā)展的同時也帶來了跨區(qū)域監(jiān)管難題。浙江省藥監(jiān)局聚焦監(jiān)管痛點����,帶領(lǐng)紹興市市場監(jiān)管局創(chuàng)新開發(fā)“醫(yī)療器械跨區(qū)域監(jiān)管平臺”,以數(shù)字化手段推動線上線下一體化治理��,促進各地監(jiān)管責任落實�,實現(xiàn)跨區(qū)域協(xié)同高效檢查,服務(wù)全國統(tǒng)一大市場建設(shè)�����。
??? 隨著2021年醫(yī)療器械注冊人制度的全面實施�,醫(yī)療器械跨區(qū)域委托生產(chǎn)逐漸成為常態(tài),在極大促進產(chǎn)業(yè)發(fā)展的同時也帶來了跨區(qū)域監(jiān)管難題��。浙江省藥監(jiān)局聚焦監(jiān)管痛點����,帶領(lǐng)紹興市市場監(jiān)管局創(chuàng)新開發(fā)“醫(yī)療器械跨區(qū)域監(jiān)管平臺”,以數(shù)字化手段推動線上線下一體化治理�,促進各地監(jiān)管責任落實�,實現(xiàn)跨區(qū)域協(xié)同高效檢查�����,服務(wù)全國統(tǒng)一大市場建設(shè)�。
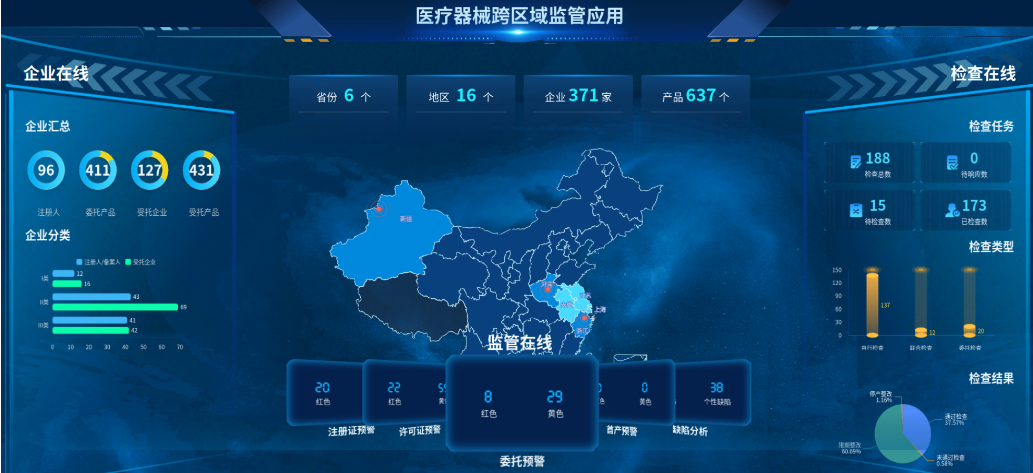
??? 一是暢通跨省數(shù)據(jù)互聯(lián)渠道。針對醫(yī)療器械跨省關(guān)聯(lián)企業(yè)海量數(shù)據(jù)互聯(lián)互通難題����,平臺通過集成化數(shù)據(jù)打包,建立數(shù)據(jù)信息庫��,歸集主體登記��、產(chǎn)品質(zhì)量�、行政處罰、不合格報告��、不良事件監(jiān)測等信息數(shù)據(jù)�,向?qū)俚乇O(jiān)管部門開放數(shù)據(jù)端口,有效打破數(shù)據(jù)流通壁壘�����,為屬地監(jiān)管部門掌握企業(yè)全貌提供數(shù)據(jù)支撐,實現(xiàn)“數(shù)據(jù)跑”代替“人工跑”�����。截至目前����,平臺歸集上海、江蘇�、浙江、安徽����、河南、新疆等6?。ㄗ灾螀^(qū)�����、直轄市)醫(yī)療器械注冊申請人信息209家���、受托生產(chǎn)企業(yè)信息184家����,包含委托生產(chǎn)產(chǎn)品418件、受托生產(chǎn)產(chǎn)品437件���。

??? 二是打造跨省報告互認模式�����。監(jiān)管標準不統(tǒng)一��、檢查報告不互認是實現(xiàn)跨區(qū)域監(jiān)管的核心難題��。平臺以開放數(shù)據(jù)端口為基礎(chǔ)��,科學設(shè)置報告上傳��、共享查詢�����、數(shù)據(jù)統(tǒng)計等功能�����,確保不同區(qū)域的監(jiān)管人員能實時上傳��、查閱���、統(tǒng)計相關(guān)醫(yī)療器械企業(yè)的檢查報告。同時,通過配置后臺權(quán)限�,系統(tǒng)可根據(jù)檢查人員的實際需求設(shè)置共享權(quán)限,有效保護企業(yè)數(shù)據(jù)安全�。截至目前����,通過聯(lián)合檢查��、委托檢查���、自行檢查��,形成檢查報告174份�,涉及企業(yè)100余家。
??? 三是探索跨省檢查隊伍建設(shè)�����。2021年����,浙江紹興聯(lián)合新疆博州�、河南許昌成立全國首個醫(yī)療器械跨區(qū)域監(jiān)管聯(lián)盟,組建首支醫(yī)療器械跨區(qū)域監(jiān)管檢查員隊伍����。2024年�����,隨著上海、江蘇��、浙江����、安徽、河南�����、新疆等“6省先試”�,醫(yī)療器械跨區(qū)域監(jiān)管檢查員隊伍已成長為一支242人、包含6?��。ㄗ灾螀^(qū)�����、直轄市)醫(yī)療器械監(jiān)管業(yè)務(wù)骨干的高素質(zhì)檢查員隊伍����,并在不斷協(xié)同合作中形成了信息互通�����、人員互派����、結(jié)果互認的“三互”機制,醫(yī)療器械跨區(qū)域監(jiān)管效能持續(xù)深化���。
??? 下一步���,浙江省藥監(jiān)局將按照國家藥監(jiān)局工作要求,繼續(xù)深化跨區(qū)域監(jiān)管模式探索����,推動數(shù)據(jù)流動“橫向”跨區(qū)域、“縱向”跨層級�����,持續(xù)擴大應(yīng)用使用領(lǐng)域和覆蓋面���,讓實踐成果在更大范圍共享����,為促進醫(yī)療器械行業(yè)高質(zhì)量發(fā)展提供堅實數(shù)字底座�����。